国家药品不良反应监测年度报告(2020年)
时间:2021-04-08来源:国家药品监督管理局药品评价中心
为全面反映2020年我国药品不良反应监测情况,提高安全用药水平,更好地保障公众用药安全,国家药品不良反应监测中心组织编撰《国家药品不良反应监测年度报告(2020年)》。
第1章 药品不良反应监测工作情况
2020年,面对突如其来的新冠肺炎疫情,全国各级药品不良反应监测机构上下同心,全力以赴,按照习近平总书记对食品药品“四个最严”要求,药品不良反应监测评价工作平稳有序开展,法规制度不断完善,监测评价体系逐步健全,报告数量和质量稳步提升,风险控制手段更加成熟,各项工作取得明显成效,为药品监管提供了科学有力支撑。
一是强化顶层设计,规划体系能力建设目标。发布《关于进一步加强药品不良反应监测评价体系和能力建设的意见》,明确“十四五”期间监测评价体系和能力建设的六项目标、九项任务和三项保障,加快完善监测评价制度体系,不断提高监测评价能力。
二是落实法规要求,推动配套技术规范出台。发布《药物警戒委托协议撰写指导原则(试行)》,起草《药物警戒质量管理规范》,指导药品上市许可持有人(以下简称持有人)开展监测、报告、分析和评价工作,推动药物警戒制度建立健全。
三是科学分析评价,充分发挥技术支撑作用。密切关注国内外监管动态,强化监测数据分析评价。根据评价结果,及时发布药品安全警示信息。2020年发布注销安乃近注射液等品种药品注册证书公告共3期,发布药品说明书修订公告共47期。
四是有效监测风险,保障疫情防控用药安全。面对疫情,全国各级监测机构迅速响应,密切跟进《新型冠状病毒肺炎诊疗方案》所列药品,重点关注相关预警信号、群体事件及药品不良反应报告情况,全面加强新冠肺炎防控及治疗药品监测、分析和评价,切实保障疫情防控用药安全。
五是升级信息系统,助力监测评价工作发展。加快转化实施ICH E2B(R3)数据标准,建成兼容在线报告、网关传输、XML文件递交多种报告途径的药品上市许可持有人直报系统。继续加强与医疗机构的合作,迄今为止,已在全国366家三级医疗机构建立药品不良反应监测哨点。
第2章 药品不良反应/事件报告情况
2.1 报告总体情况
2.1.1 2020年度药品不良反应/事件报告情况
2020年全国药品不良反应监测网络收到《药品不良反应/事件报告表》167.6万份。1999年至2020年,全国药品不良反应监测网络累计收到《药品不良反应/事件报告表》1,687万份(图1)。
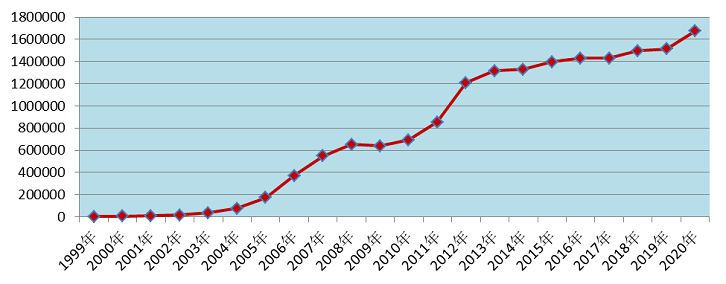
图1 1999年-2020年全国药品不良反应/事件报告数量增长趋势
2.1.2 新的和严重药品不良反应/事件报告情况
2020年全国药品不良反应监测网络收到新的和严重药品不良反应/事件报告50.6万份;新的和严重药品不良反应/事件报告占同期报告总数的30.2%。
2020年全国药品不良反应监测网络收到严重药品不良反应/事件报告16.7万份,严重药品不良反应/事件报告占同期报告总数的10.0%(图2)。

图2 2004年-2020年新的和严重以及严重药品不良反应/事件报告比例
小贴士:
如何认识药品不良反应报告?
药品不良反应是指合格药品在正常用法用量下出现的与用药目的无关的有害反应。药品不良反应是药品的固有属性,一般来说,所有药品都会存在或多或少、或轻或重的不良反应。
药品不良反应监测是药品上市后安全监管的重要支撑,其目的是及时发现和控制药品安全风险。持有人、经营企业、医疗机构应当报告所发现的药品不良反应,国家鼓励公民、法人和其他组织报告药品不良反应。
经过各方努力,持有人、经营企业、医疗机构报告药品不良反应的积极性已经逐步提高,我国药品不良反应报告数量总体呈上升趋势。严重药品不良反应/事件报告比例是衡量报告总体质量和可利用性的重要指标之一,药品不良反应监测评价工作一直将收集和评价新的和严重反应作为重点内容。新的和严重药品不良反应报告,尤其是严重药品不良反应报告数量多了,并非说明药品安全水平下降,而意味着监管部门掌握的信息越来越全面,对药品的风险更了解,风险更可控,对药品的评价更加有依据,监管决策更加准确。同样,在医疗实践中,能及时了解药品不良反应发生的表现、程度,并最大限度地加以避免,也是保证患者用药安全的重要措施。
2.1.3 每百万人口平均报告情况
每百万人口平均报告数量是衡量一个国家药品不良反应监测工作水平的重要指标之一。2020年我国每百万人口平均报告数为1,251份。
2.1.4 药品不良反应/事件县级报告比例
药品不良反应/事件县级报告比例是衡量我国药品不良反应监测工作均衡发展及覆盖程度的重要指标之一。2020年全国98.3%的县级地区报告了药品不良反应/事件。
2.1.5 药品不良反应/事件报告来源
持有人、经营企业和医疗机构是药品不良反应报告的责任单位。按照报告来源统计,2020年来自医疗机构的报告占85.4%;来自经营企业的报告占10.6%;来自持有人的报告占3.9%;来自个人及其他报告者的报告占0.1%(图3)。
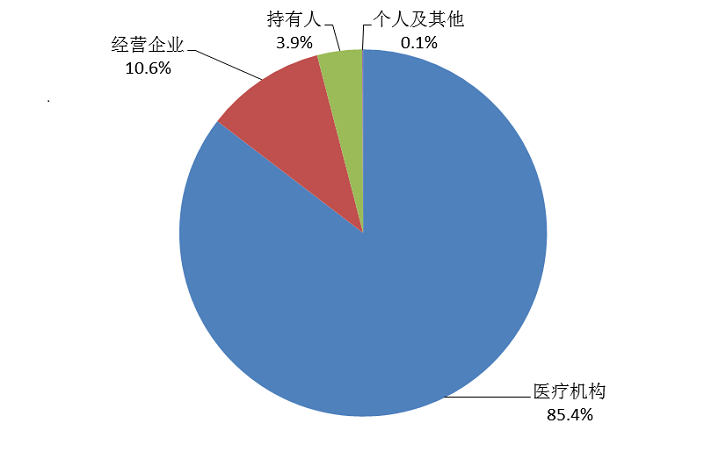
图3 2020年药品不良反应/事件报告来源
2.1.6 报告人职业
按照报告人职业统计,医生占55.3%,药师占24.7%,护士占13.7%,其他职业占6.3%(图4)。
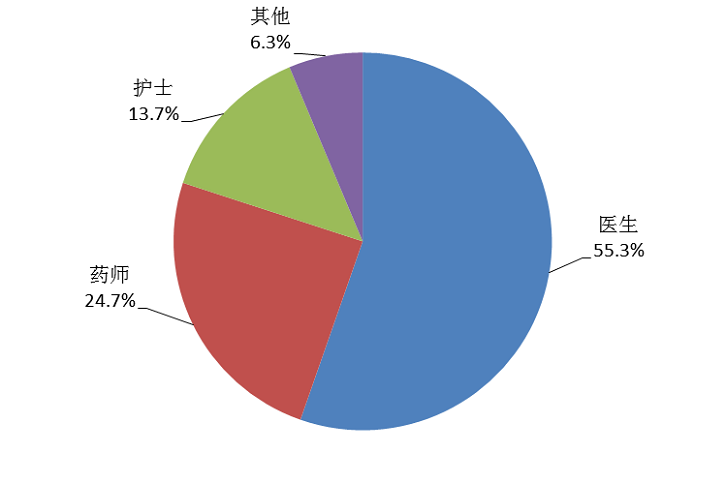
图4 2020年报告人职业构成
2.1.7 药品不良反应/事件报告涉及患者情况
2020年药品不良反应/事件报告中,男女性别比为0.87:1,女性略多于男性。从年龄分布看,14岁以下儿童占7.7%,65岁及以上老年患者占30.3%(图5)。
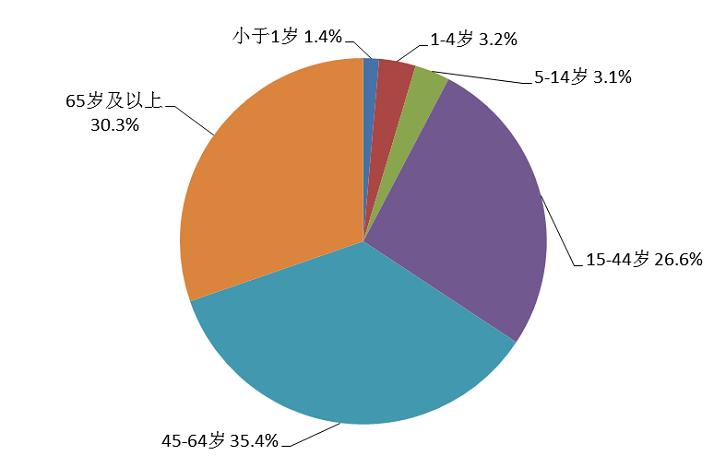
图5 2020年药品不良反应/事件报告涉及患者年龄
2.1.8 药品不良反应/事件报告涉及药品情况
按照怀疑药品类别统计,化学药品占83.0%、中药占13.4%、生物制品占1.1%、无法分类者占2.5%(图6)。
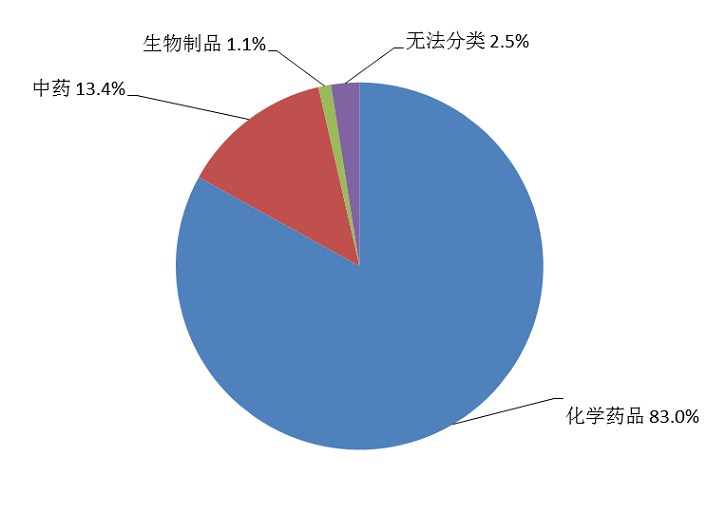
图6 2020年药品不良反应/事件报告涉及药品类别
按照给药途径统计,2020年药品不良反应/事件报告中,注射给药占56.7%、口服给药占38.1%、其他给药途径占5.2%。注射给药中,静脉注射给药占91.1%、其他注射给药占8.9%(图7)。

图7 2020年药品不良反应/事件报告涉及给药途径
2.1.9 药品不良反应/事件累及器官系统情况
2020年报告的药品不良反应/事件中,累及器官系统排名前3位依次为胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应。

图8 2020年药品不良反应/事件累及器官系统
2.2 基本药物监测情况
2.2.1 国家基本药物监测总体情况
2020年全国药品不良反应监测网络共收到《国家基本药物目录(2018年版)》收载品种的不良反应/事件报告83.0万份,其中严重报告8.8万份,占10.6%。报告涉及化学药品和生物制品占88.1%,中成药占11.9%。
2.2.2 国家基本药物化学药品和生物制品情况分析
《国家基本药物目录(2018年版)》化学药品和生物制品部分共417个(类)品种。2020年全国药品不良反应监测网络共收到国家基本药物化学药品和生物制品药品不良反应/事件报告78.1万例次,其中严重报告10.4万例次,占13.4%。
2020年国家基本药物化学药品和生物制品不良反应/事件报告按照药品类别统计,报告数量排名前5位的分别是抗微生物药、心血管系统用药、抗肿瘤药、激素及影响内分泌药、治疗精神障碍药;累及器官系统排名前5位的是胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应、各类神经系统疾病以及各类检查。
2.2.3 国家基本药物中成药情况分析
《国家基本药物目录(2018年版)》中成药共涉及268个品种。2020年全国药品不良反应监测网络收到国家基本药物中成药不良反应/事件报告10.5万例次,其中严重报告6,358例次,占6.0%。2020年国家基本药物7大类中成药中,药品不良反应/事件报告总数由多到少依次为内科用药、骨伤科用药、妇科用药、外科用药、耳鼻喉科用药、儿科用药、眼科用药。
以上监测数据表明,2020年国家基本药物监测总体情况基本保持平稳。
小贴士:
《国家基本药物目录(2018年版)》收录品种情况
2018年11月1日起,我国正式启用《国家基本药物目录(2018年版)》。该目录主要分为化学药品和生物制品、中成药和中药饮片三个部分。其中化学药品和生物制品部分包括抗微生物药、抗寄生虫病药、麻醉药等26类药品,中成药部分包括内科用药、外科用药、妇科用药等7类药品。与2012年版基药目录相比,2018年版基药目录共调入药品187种,调出22种(其中17个为化药),目录总品种数量由原来的520种增加到685种,其中西药417种、中成药268种。
2.3 化学药品、生物制品监测情况
2.3.1 总体情况
2020年药品不良反应/事件报告中,涉及怀疑药品179.8万例次,其中化学药品占83.0%,生物制品占1.1%。2020年严重不良反应/事件报告涉及怀疑药品21.3万例次,其中化学药品占90.3%,生物制品占1.2%。
2.3.2 涉及患者情况
2020年化学药品、生物制品不良反应/事件报告中,男女患者比为0.86:1,女性多于男性。14岁以下儿童患者的报告占7.7%,65岁及以上老年患者的报告占30.9%。
2.3.3 涉及药品情况
2020年药品不良反应/事件报告涉及的化学药品中,例次数排名前5位的类别依次为抗感染药、心血管系统用药、肿瘤用药、电解质/酸碱平衡及营养药、神经系统用药。2020年严重药品不良反应/事件涉及化学药品中,报告数量最多的为肿瘤用药,占32.2%;其次是抗感染药,占28.3%。按严重报告占本类别报告比例计算,肿瘤用药的严重报告比例最高,为41.5%,其次是免疫系统用药,为21.4%。
2020年药品不良反应/事件报告涉及的生物制品中,抗毒素及免疫血清占37.8%,细胞因子占27.7%,血液制品占4.9%。
按剂型统计,2020年化学药品不良反应/事件报告中,注射剂、口服制剂所占比例分别为60.4%和35.0%,其他剂型占4.6%。生物制品中,注射剂、口服制剂占比分别为94.4%和0.3%,其他制剂占5.3%。
2.3.4 总体情况分析
2020年化学药品和生物制品不良反应/事件报告情况与2019年基本一致。从不良反应涉及患者年龄看,14岁以下儿童占比较2019年明显降低,提示儿童用药的安全性总体良好;65岁及以上老年患者占比持续升高,提示临床应加大对老年患者安全用药的管理。从药品类别上看,抗感染药报告数量依然居于首位,但占比已连续9年呈下降趋势,反映出临床抗感染药的使用日趋合理;肿瘤用药占比依然呈上升趋势,其严重报告构成比居于首位,提示肿瘤用药的安全性风险需持续关注。从药品剂型上看,化学药品和生物制品报告中注射剂占比均出现较明显下降,与总体报告中注射剂不良反应的下降趋势基本一致。
小贴士:
什么是药物相互作用?
药物与药物之间的相互作用,是指两种或两种以上药物同时或先后序贯应用时,药物之间的相互影响和干扰可改变药物的体内过程及机体对药物的反应性,从而使药物的药理效应或毒性发生变化。药物的相互作用包括两个方面:一是不影响药物在体液中的浓度但改变药理作用,使原有的效应增强或减弱;二是通过药物的吸收、分布、代谢和排泄,改变药物在作用部位的浓度而影响药物作用。引起药物相互作用的因素较多,一些弱酸性或弱碱性药物可能改变体内pH值,从而影响其他药物的解离度,如抗酸药奥美拉唑可以与酮康唑等药物发生相互作用;一些药物可以抑制肝脏药物代谢酶,减慢其他药物的代谢,如西咪替丁可以与华法林等药物发生相互作用;一些药物可能与其他药物竞争结合受体,导致其他药物的治疗作用增强或减弱,如普萘洛尔可以与异丙肾上腺素等药物发生相互作用。药物相互作用情况,可以参见药品说明书中【药物相互作用】项下的内容。患者应养成记录自己使用药物的习惯,看医生或去药店购买药品时,准确告诉医生和药师目前正在使用的药物;用药前详细阅读药品说明书,如果有疑问应及时咨询医生或药师。
2.4 中药监测情况
2.4.1 总体情况
2020年药品不良反应/事件报告中,涉及怀疑药品179.8万例次,其中中药占13.4%;2020年严重不良反应/事件报告涉及怀疑药品21.3万例次,其中中药占6.3%。
2.4.2 涉及患者情况
2020年中药不良反应/事件报告中,男女患者比为0.82:1。14岁以下儿童患者占6.0%,65岁及以上老年患者占28.1%。
2.4.3 涉及药品情况
2020年药品不良反应/事件报告涉及的中药中,例次数排名前5位的类别分别是理血剂中活血化瘀药(25.8%)、清热剂中清热解毒药(11.9%)、祛湿剂中清热除湿药(6.5%)、补益剂中益气养阴药(5.7%)、祛湿剂中祛风胜湿药(4.6%)。2020年中药严重不良反应/事件报告的例次数排名前5位的类别分别是理血剂中活血化瘀药(41.2%)、补益剂中益气养阴药(12.7%)、开窍剂中凉开药(7.9%)、清热剂中清热解毒药(7.3%)、祛湿剂中清热除湿药(3.0%)。
2020年中药不良反应/事件报告按照给药途径统计,注射给药占33.3%、口服给药占56.4%、其他给药途径占10.3%。注射给药中,静脉注射给药占97.8%、其他注射给药占2.2%。
2.4.4 总体情况分析
与2019年相比,2020年中药不良反应/事件报告数量有所上升,但严重报告占比有所下降。从给药途径看,注射给药占比下降较为明显。从药品类别上看,活血化瘀药的报告数量依然居首位,但占比略有下降。从总体情况看,2020年中药占总体不良反应/事件报告比例呈下降趋势,但仍需要注意安全用药。
小贴士:
为什么中药会引起不良反应?
中药和其他药品一样,也可能会产生不良反应。辨证论治是中医认识疾病和治疗疾病的基本原则,中药的使用讲究合理组方、一人一方、随证加减,有时还存在讲究道地药材、如法炮制等。严格地说,在这样的情况下服用中药,有助减少和避免不良反应/事件。但是如果不遵守辩证论治的原则或者辩证不当,组方不合理,将引发更多不良反应/事件。现在许多中成药、中药新剂型在使用过程中,不良反应也很多,应该引起重视。
第3章 相关风险控制措施
根据2020年药品不良反应监测数据和分析评价结果,国家药品监督管理局对发现存在安全隐患的药品及时采取相应风险控制措施,以保障公众用药安全。
发布关于注销安乃近注射液等品种、含磺胺二甲嘧啶制剂、羟布宗片药品注册证书的公告共3期。
发布甲磺酸阿帕替尼片、银杏叶片、复方甘草片等药品说明书修订公告共47期,增加或完善57个(类)品种说明书中的警示语、不良反应、注意事项、禁忌等安全性信息。
发布《药物警戒快讯》12期,报道国外药品安全信息61条。
第4章 各论
根据药品不良反应监测结果以及公众关注情况,对抗感染药、心血管系统用药、诊断用药、注射剂、老年人用药的不良反应报告情况进行分析,并提示安全风险如下:
4.1 关注抗感染药用药风险
抗感染药是指具有杀灭或抑制各种病原微生物作用的药品,包括抗生素、合成抗菌药、抗真菌药、抗病毒药等,是临床应用最为广泛的药品类别之一,其不良反应/事件报告数量一直居于首位,是药品不良反应监测工作关注的重点。
2020年全国药品不良反应监测网络共收到抗感染药不良反应/事件报告49.5万份,其中严重报告4.9万份,占9.8%。抗感染药不良反应/事件报告占2020年总体报告的29.5%。
4.1.1 涉及药品情况
2020年抗感染药不良反应/事件报告数量排名前3位的药品类别分别是头孢菌素类、喹诺酮类、青霉素类,严重不良反应/事件报告数量排名前3位的药品类别分别是头孢菌素类、喹诺酮类、抗结核病药。
2020年抗感染药不良反应/事件报告中,注射剂占76.0%,口服制剂占20.3%,其他剂型占3.7%;与药品总体报告剂型分布相比,注射剂比例偏高。严重不良反应/事件报告中,注射剂占78.8%,口服制剂占20.2%,其他剂型占1.0%。
4.1.2 累及器官系统情况
2020年抗感染药不良反应/事件报告中,整体报告和严重报告的药品不良反应/事件累及器官系统情况详见图9。与抗感染药的整体报告相比,严重报告的全身性疾病及给药部位各种反应、免疫系统疾病、呼吸系统、胸及纵隔疾病、各类检查构成比明显偏高。
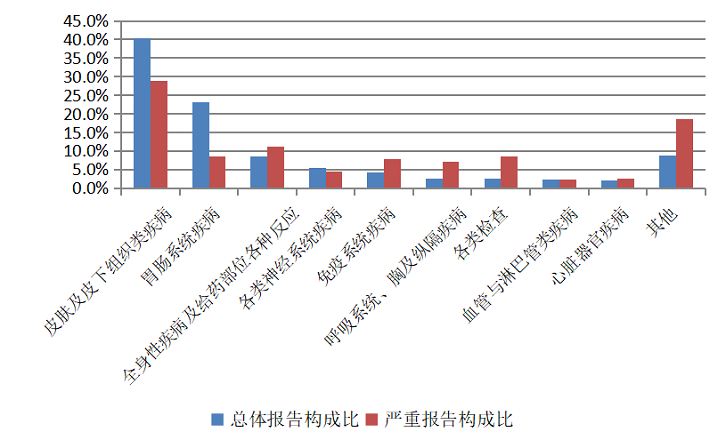
图9 2020年抗感染药不良反应/事件累及器官系统
抗感染药整体药品不良反应/事件报告中,口服制剂累及器官系统排名前5位的是胃肠系统疾病、皮肤及皮下组织类疾病、各类神经系统疾病、肝胆系统疾病、全身性疾病及给药部位各种反应;注射剂累及器官系统排名前5位是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应、各类神经系统疾病、免疫系统疾病。
抗感染药严重药品不良反应/事件报告中,口服制剂累及器官系统排名前5位是皮肤及皮下组织类疾病、肝胆系统疾病、各类检查、胃肠系统疾病、代谢及营养类疾病;注射剂累及器官系统排名前5位是皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应、免疫系统疾病、呼吸系统、胸及纵隔疾病、胃肠系统疾病。
4.1.3 监测情况分析及安全风险提示
近年来,抗感染药不良反应/事件报告占总体报告比例呈现持续下降趋势,说明国家加强抗感染药使用管理等措施取得一定实效,但其严重不良反应报告数量仍然很高,提示抗感染药的用药风险仍需继续关注。
小贴士:
阿米卡星的严重不良反应主要有哪些?
阿米卡星是一种氨基糖苷类抗生素,是2018年版国家基本药物目录品种。和所有的氨基糖苷类药物一样,阿米卡星也有潜在的耳毒性、肾毒性以及神经肌肉毒性。耳毒性主要是对第八脑神经的毒性作用,会导致听觉丧失、平衡失调或者两者同时发生。在肾损害患者中,氨基糖苷类药物出现神经毒性的风险性更大。高频耳聋通常最先出现,并且仅能够通过听觉测试检查出来。神经毒性的其他表现还有麻木、皮肤针刺感、肌肉抽搐和惊厥等。氨基糖苷药物的耳毒性通常是不可逆的。肾毒性主要表现是肾功能不全,严重的可导致急性肾损伤。神经肌肉毒性主要是急性肌肉麻痹和呼吸暂停。阿米卡星注射剂还有发生严重过敏反应的风险,包括过敏性休克,严重者可导致死亡。使用阿米卡星时请仔细阅读药品说明书,对于接受阿米卡星的患者需要进行密切临床观察。
4.2 关注心血管系统用药风险
心血管系统用药是指用于心脏疾病治疗、血管保护、血压和血脂调节的药品,包括降血压药、抗心绞痛药、血管活性药、抗动脉粥样硬化药、抗心律失常药、强心药和其他心血管系统用药。近年来,心血管系统用药不良反应/事件报告数量及严重报告占比均呈现上升趋势,提示应对该类药品风险给予更多关注。
2020年全国药品不良反应监测网络共收到心血管系统用药的不良反应/事件报告15.7万份,占总体报告的9.3%;其中严重报告9,008份,占5.7%。
4.2.1 涉及患者情况
按性别统计,2020年心血管系统用药不良反应/事件报告中,女性患者比男性患者高2.6个百分点;严重报告中,男性患者比女性患者高2.1个百分点。
按年龄统计,2020年心血管系统用药不良反应/事件报告中,45-64岁与65岁及以上年龄组分别占43.5%和46.6%(图10),远高于其他年龄组比例;严重报告中,65岁及以上年龄组占52.4%。
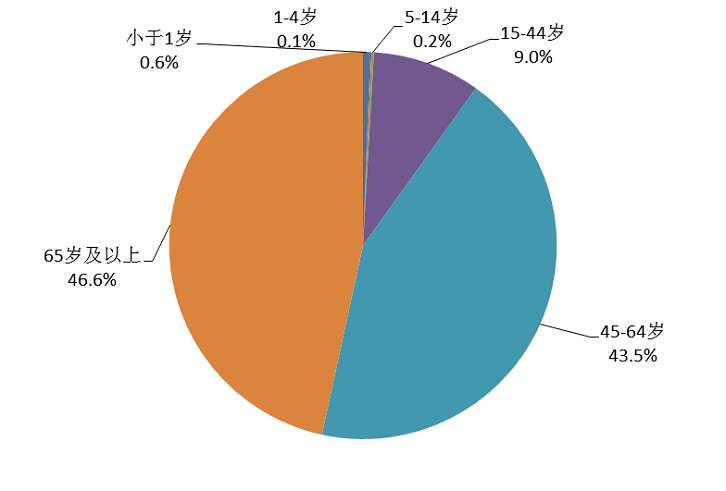
图10 2020年心血管系统用药不良反应/事件报告涉及患者年龄
4.2.2 涉及药品情况
2020年心血管系统用药不良反应/事件报告数量排名前3位的药品类别是降血压药、抗心绞痛药、抗动脉粥样硬化药;心血管系统用药严重报告数量排名前3位的药品类别是抗动脉粥样硬化药、降血压药、抗心绞痛药。
2020年心血管系统用药不良反应/事件报告中,注射剂占29.0%,口服制剂占70.1%,其他剂型占0.9%;严重报告中,注射剂占44.1%,口服制剂占55.4%,其他剂型占0.5%。
4.2.3 累及器官系统情况
2020年心血管系统用药不良反应/事件报告中,口服制剂累及器官系统排名前5位是肝胆系统疾病、各类检查、各类神经系统疾病、全身性疾病及给药部位各种反应、皮肤及皮下组织类疾病;注射剂累及器官系统前5位是全身性疾病及给药部位各种反应、各类神经系统疾病、皮肤及皮下组织类疾病、心脏器官疾病、呼吸系统、胸及纵隔疾病(图11)。
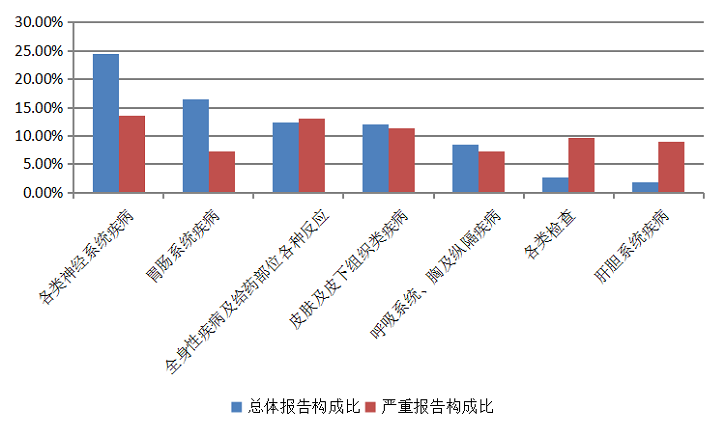
图11 2020年心血管系统用药不良反应/事件累及器官系统
4.2.4 监测情况分析及安全风险提示
统计分析结果显示,心血管系统用药不良反应/事件报告中,65岁及以上年龄组患者报告占比及严重报告占比均明显高于总体报告中该年龄组患者水平,提示老年患者是心血管系统用药的主要群体,医务人员和患者应关注发生严重不良反应的风险。
2020年心血管系统用药不良反应/事件报告中,口服制剂的报告占比明显高于注射剂,提示心血管系统用药不良反应/事件报告更多来自口服给药途径,同时不除外与疫情期间患者的诊治方式发生变化有关。口服制剂中,硝苯地平不良反应/事件报告数量最多。这可能与高血压患者需要长期用药,使用较多有关;严重不良反应/事件报告中,他汀类药品报告数量最多。这可能与他汀类药品使用较多有关,他汀类药品除用于血脂代谢紊乱及相关心血管疾病的治疗,还用于此类疾病的预防;此外,不排除其中存在的不合理、不规范使用情况,提示医务人员和患者应关注此类药品的风险。
小贴士 :
患者使用降血压药类药品应注意什么?
降压药物为处方药,使用需要医生诊断和处方。降血压药类药品包括血管扩张类降压药、肾素-血管紧张素系统抑制药、利尿性降压药、交感神经抑制药、钙通道阻滞药等。此类药品严重不良反应主要表现为头痛、肝功能异常、胸部不适、头晕、呼吸困难、恶心、低血压、寒战等。不同类别降压药物的不良反应存在差异,患者在使用此类药品前应仔细阅读药品说明书不良反应、注意事项、警示、禁忌等安全性提示信息,服药时应注意以下几点:1.明确所服用高血压药的剂量及服用时间;2.从小剂量开始服用,不要随意加大剂量或减少剂量,严格按照医嘱服药;3.高血压患者需要终生服用药物;4.老年人降压切忌过快、过低,应结合原来的血压水平,将其控制在合理范围;5.在服药过程中如出现不适,应及时与医生或药师联系,避免发生严重不良反应。
4.3 关注诊断用药风险
诊断用药可分为医学影像学检查对比剂、器官功能检查用药以及其他诊断用药。临床使用较为广泛的诊断用药有40多个品种,以医学影像检查中使用的对比剂为主,其种类较多,常用的有用于心血管造影的含碘对比剂、用于磁共振的含钆对比剂以及消化道造影的硫酸钡等。近年来,含碘、含钆对比剂的相关风险有所增加,提示应对该类药品风险给予关注。
2020年全国药品不良反应监测网络共收到诊断用药的不良反应/事件报告1.7万份,占总体报告的1.0%;其中严重报告2,934份,占17.2%。
4.3.1 涉及患者情况
按性别统计,2020年诊断用药不良反应/事件报告中,男性患者比女性患者高7.9个百分点;严重报告中,男性患者比女性患者高4.6个百分点。
按年龄统计,2020年诊断用药不良反应/事件报告中,14岁以下年龄组占1.1%,15-44岁年龄组占18.7%,45-64岁与65岁及以上年龄组分别占50.2%和30.0%,高于其他年龄组比例;严重报告中,45-64岁与65岁及以上年龄组分别占48.0%和34.1%。
4.3.2 涉及药品情况
2020年诊断用药不良反应/事件报告数量排名前3位的药品是碘克沙醇、碘海醇、碘佛醇(图12);诊断用药严重报告数量排名前3位的药品是碘克沙醇、碘海醇、碘佛醇。

图12 2020年诊断用药不良反应/事件涉及药品
4.3.3 累及器官系统情况
2020年诊断用药严重不良反应/事件报告累及器官系统排名前5位的是皮肤及皮下组织类疾病、免疫系统疾病、全身性疾病及给药部位各种反应、呼吸系统、胸及纵隔疾病、各类神经系统疾病(图13)。诊断用药严重不良反应/事件报告中,不良反应主要表现为皮疹、过敏性休克、瘙痒症、类速发严重过敏反应、呼吸困难、超敏反应、胸部不适、血压降低等。
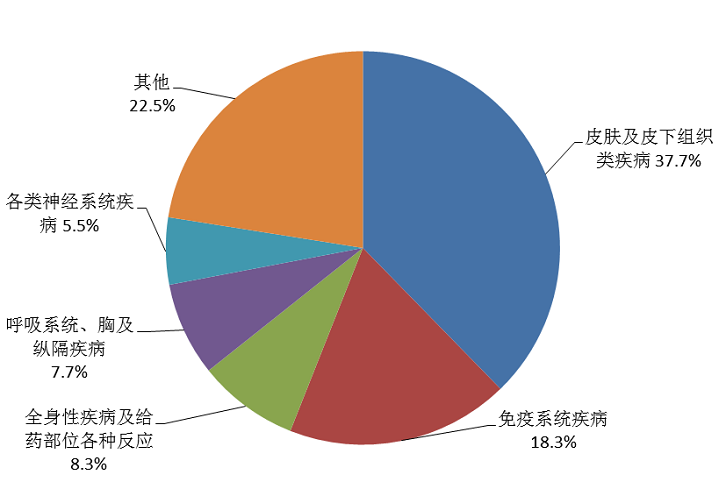
图13 2020年诊断用药严重药品不良反应/事件报告累及器官系统
4.3.4 监测情况分析及安全风险提示
2020年诊断用药不良反应/事件报告总数排名前10位品种主要为含碘对比剂和含钆对比剂,严重不良反应/事件报告与以上情况相似,其中含钆对比剂报告数量占比略有上升。2020年诊断用药严重不良反应/事件报告相比于整体报告,免疫系统疾病和呼吸系统、胸及纵隔疾病排名上升,报告数占比增加。
诊断用药不良反应/事件报告中,45岁及以上年龄组患者报告占比在80%以上,提示中老年患者是诊断用药使用后产生不良反应的主要群体,医务人员和患者应关注该群体发生严重不良反应的风险。
使用含碘或含钆对比剂的患者发生的过敏性休克等严重不良反应,时间过程通常比较短,抢救不及时甚至有致命危险。对过敏性休克等严重反应要着重于严密观察、及早发现并及时处理。造影检查室内要配备各种处理和抢救的药品和器械,要有掌握处理技能的医护人员在场。同时,为进一步保障公众用药安全,生产企业应加强含碘、含钆对比剂的上市后安全性监测与研究,并及时将产品安全性信息传达给医务人员及患者。
小贴士:
目前国内上市的含碘、含钆对比剂有哪些?有哪些严重不良反应?
对比剂种类多样,产品也不断在更新换代。目前国内上市的含碘对比剂主要包括碘海醇注射液、碘美普尔注射液、碘佛醇注射液、碘帕醇注射液、碘普罗胺注射液、碘克沙醇注射液、碘比醇注射液、碘克沙酸葡胺钠注射液、泛影葡胺注射液和复方泛影葡胺注射液。国内上市的含钆对比剂主要包括有钆喷酸葡胺注射液、钆双胺注射液、钆贝葡胺注射液、钆塞酸二钠注射液、钆特酸葡胺注射液、钆特醇注射液、钆布醇注射液。此类药品严重不良反应主要表现为皮疹、过敏性休克、瘙痒症、类速发严重过敏反应、呼吸困难、超敏反应等。
使用含碘、含钆对比剂应注意什么?
医务人员及患者应仔细阅读药品说明书不良反应、注意事项、警示、禁忌等安全性提示信息;患者在检查过程中,对个人健康状况有疑问时,应及时询问医务人员。使用含碘、含钆对比剂过程中,要严密观察、及早发现并及时处理出现的严重不良反应。造影检查室内要配备各种处理和抢救的药品和器械,要有掌握处理技能的医护人员在场。公众还可从国家药品监督管理局(www.nmpa.gov.cn)及国家药品不良反应监测中心(www.cdr-adr.org.cn)官方网站,查询到国家近年来发布的针对含碘、含钆对比剂相关风险的提示信息。
4.4 关注注射剂用药风险
2020年注射剂(不含疫苗)不良反应/事件与2019年同期相比,总体报告数小幅下降,严重报告数小幅增长。按照剂型统计,2020年药品总体不良反应/事件报告中注射剂(不含疫苗)占57.0%,严重报告中注射剂(不含疫苗)占73.0%。按药品分类统计,注射剂(不含疫苗)总体报告中化学药品注射剂占88.1%,中药注射剂占7.8%,生物制品占1.5%,无法分类者占2.6%;注射剂(不含疫苗)严重报告中化学药品注射剂占90.4%,中药注射剂占6.1%,生物制品占1.4%,无法分类者占2.1%。
4.4.1 药品情况
化学药品注射剂报告数量排名前3位的药品类别是抗感染药,肿瘤用药,电解质、酸碱平衡及营养药(图14)。
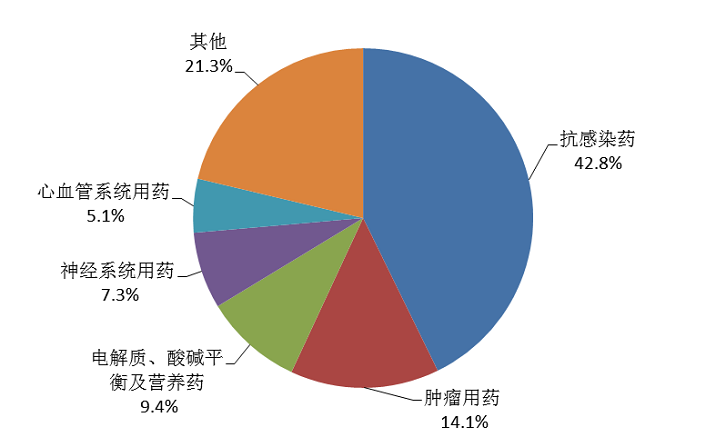
图14 2020年化学药品注射剂不良反应/事件报告涉及药品类别
中药注射剂总体报告涉及中药注射剂类别排名前5位的是理血剂、补益剂、开窍剂、清热剂、祛痰剂(图15)。
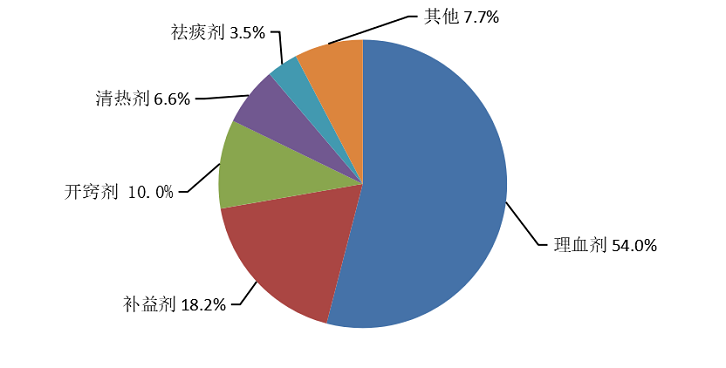
图15 2020年中药注射剂不良反应/事件报告涉及药品类别
4.4.2 累及器官系统情况
2020年注射剂总体不良反应/事件报告中,累及器官系统排名前5位的是皮肤及皮下组织类疾病、胃肠系统疾病、全身性疾病及给药部位各种反应、各类神经系统疾病和各类检查。注射剂严重不良反应/事件中,累及器官系统排名前5位的是血液及淋巴系统疾病、皮肤及皮下组织类疾病、各类检查、全身性疾病及给药部位各种反应和胃肠系统疾病(图16)。
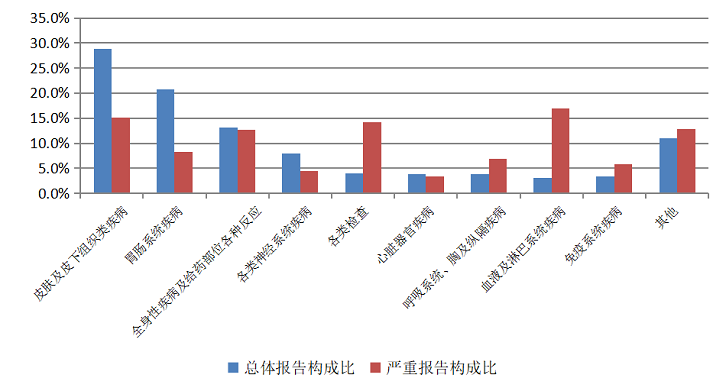
图16 2020年注射剂不良反应/事件累及器官系统
4.4.3 监测情况分析及安全风险提示
从剂型统计情况看,2020年注射剂(不含疫苗)不良反应/事件总体报告数量与2019年同期相比小幅下降,但占比仍然相对较高,与近年来总体情况基本一致。从用药人群统计情况看,儿童的注射剂(不含疫苗)不良反应/事件报告数量与2019年同期相比小幅下降,但总体占比仍相对较高。根据注射剂监测情况,建议临床医生用药前仔细阅读产品说明书,重点关注相关安全性内容,处方前进行充分的获益与风险分析,始终遵照“能吃药不打针,能打针不输液”的用药原则合理选择用药。儿童作为特殊用药人群,受脏器发育尚未完全等因素影响,对药物更为敏感,耐受性较差,更应谨慎用药。
小贴士:
怎样合理选择给药途径?
临床上给药途径多种多样,主要包括经胃肠道给药途径和非经胃肠道给药途径。经胃肠道给药途径,即口服给药途径,常见剂型如片剂、颗粒剂、胶囊剂、散剂、溶液剂、丸剂等;非经胃肠道给药途径,即除口服给药途径以外的所有其他途径,如注射给药、呼吸道给药、皮肤给药等,常见剂型如注射剂、喷雾剂、外用溶液剂、滴眼剂、栓剂等。其中,注射给药途径包括皮下注射、皮内注射、肌内注射、静脉注射等。不同给药途径具有不同的临床意义,如口服给药途径,是最常用,相对安全、方便、经济的给药途径;注射给药途径,优点是吸收快,药量准确可控,缺点是未经过人体的天然屏障,直接进入体内,可引起组织损伤、疼痛、感染,甚至严重不良反应。临床上应根据用药实际,遵循“能口服给药的,不选用注射给药;能肌内注射给药的,不选用静脉注射或滴注给药”的原则,合理选择给药途径。
4.5 关注老年人用药安全
2020年全国药品不良反应监测网络中65岁及以上老年患者相关报告占30.3%,较2019年略有升高。2020年共收到老年患者严重报告占老年患者报告总数的11.5%,高于2020年总体报告中严重报告比例。
4.5.1 涉及老年患者情况
2020年老年患者药品不良反应/事件报告中,男性和女性患者比例为0.97:1。65-69岁老年患者报告占33.7%,70-74岁老年患者报告占26.4%(图17)。
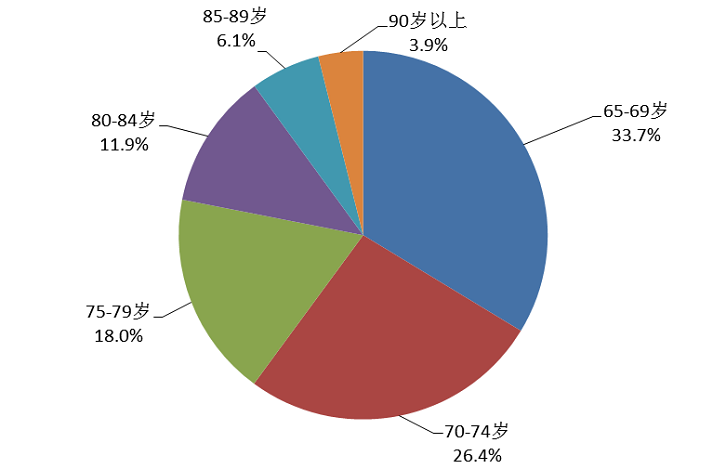
图17 2020年老年患者药品不良反应/事件涉及患者年龄
4.5.2 涉及药品情况
按照药品类别统计,化学药品占84.6%,中药占12.3%,生物制品占0.6%,无法分类者占2.5%。化学药品排名前5位的是抗感染药、心血管系统用药、肿瘤用药、神经系统用药、电解质、酸碱平衡及营养药;中药排名前5位的是理血剂、补益剂、祛湿剂、清热剂、开窍剂。
按照药品给药途径统计,注射给药占61.7%、口服给药占34.4%、其他给药途径占3.9%(图18)。注射给药中,静脉注射给药占92.7%、其他注射给药占7.3%。
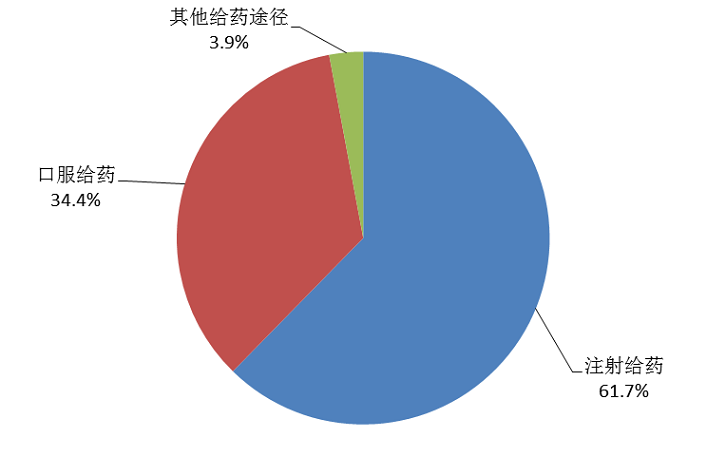
图18 2020年老年患者药品不良反应/事件涉及给药途径
4.5.3 累及器官系统情况
2020年老年患者药品不良反应/事件报告中,累及器官系统排名前5位的是胃肠系统疾病、皮肤及皮下组织类疾病、全身性疾病及给药部位各种反应、各类神经系统疾病、呼吸系统、胸及纵隔疾病,化学药品、中药累及器官系统排名前5位的与总体基本一致(图19)。

图19 2020年老年患者药品不良反应/事件累及器官系统
4.5.4 监测情况分析及安全风险提示
2020年老年患者药品不良反应/事件报告占报告总数的30.3%,老年患者严重药品不良反应/事件报告所占比例高于总体报告中严重报告的构成比,提示老年患者受基础疾病较多、机体代谢水平较差以及用药情况复杂等因素影响,发生药品不良反应的风险更大,因此仍应持续关注老年人群用药安全。
从2020年统计数据看,在药品类别分布上,老年患者用药的化学药品中,与2019年相同,心血管系统用药、神经系统用药的构成比高于该类别药品在化学药品总体报告中的构成比,提示老年患者使用以上药品较多,不良反应发生情况较多;中药排名居前的药品类别为理血剂、补益剂、祛湿剂,这3类药品的使用与老年人疾病谱和生理特点有关。
小贴士:
老年患者及家属应如何提高安全用药的认识?
我国老年人口众多,而老年人常常同时患有多种慢性疾病,随着年龄的增加,老年人罹患多种疾病和接受多种药物治疗的机会明显增加,多重用药可明显增加因药物之间相互作用所导致的药物不良反应的风险。因此应提高老年患者及家属安全用药的认识和能力,最大限度地减少药物治疗中给患者带来潜在的药源性损害,保障老年患者的用药安全。
鼓励老年患者按时门诊随访,知晓自己健康状况,一旦出现药物治疗相关的异常反应,及时就诊。建议老年患者设立个人专用药物记录本记录用药及不良反应。同时,家属需定时检查老年患者用药情况,做到按时、按医嘱规定剂量服药,要协助患者提高用药依从性和对药物的管理。老年人由于记忆力减退,容易漏服、多服、误服药物,以致难以获得疗效或加重病情。
此外,建议老年人及其家属避免随意自我药疗,不宜凭自己的经验自作主张,随便联合用药。切记不要轻信民间“偏方”、“秘方”,以免造成延误治疗或因药物间相互作用带来疗效下降或毒性增加。
第5章 有关说明
5.1 本年度报告中的数据来源于国家药品不良反应监测数据库中2020年1月1日至2020年12月31日各地区上报的数据。
5.2 与大多数国家一样,我国药品不良反应报告是通过自发报告系统收集并录入到数据库中的,存在自发报告系统的局限性,如漏报、填写不规范、信息不完善、无法计算不良反应发生率等。
5.3 每种药品不良反应/事件报告的数量受到该药品的使用量和不良反应发生率等诸多因素的影响,故药品不良反应/事件报告数量的多少不直接代表药品不良反应发生率的高低或者严重程度。
5.4 本年度报告完成时,其中一些严重报告、死亡报告尚在调查和评价的过程中,所有统计结果均为现阶段数据收集情况的真实反映,并不代表最终的评价结果。
5.5 本年度报告统计时采用监管活动医学词典(MedDRA),既往采用世界卫生组织不良反应术语集(WHO-ART)。MedDRA是在人用药品技术要求国际协调理事会(ICH)主办下编制的标准化国际医学术语集,用于与人用医疗产品相关的监管沟通和数据评估。
5.6 专业人士会分析药品与不良反应/事件的关联性,提取药品安全性风险信息,根据风险的普遍性或者严重程度,决定是否需要采取相关措施,如在药品说明书中加入安全性信息,更新药品如何安全使用的信息等。当药品的获益不再大于风险时,药品也会撤市。
5.7 本年度报告数据均来源于全国药品不良反应监测网络,不包含疫苗不良反应/事件的监测数据。

